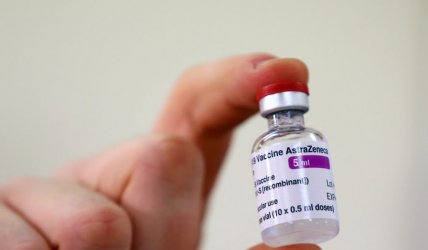
AstraZeneca може да е включила остаряла информация в доклада от изпитванията в САЩ на ваксината си, което не позволява да се придобие пълна представа за ефикасността ѝ, заяви американската здравна агенция във вторник. По-късно днес британско-шведската компания обеща до 48 часа да предостави най-актуалните си данни.
Изненадващо изразеното публично съмнение към ваксината идва след като фармацевтичната компания обяви в понеделник междинни данни, показващи по-добри от очакваните резултати при тестването ѝ в САЩ и разглеждани като научно опровержение на колебанията около препарата през последните месеци.
Независимата комисия за наблюдение на данните и безопасността (DSMB) е предупредила Националния институт по алергични и инфекциозни болести (NIAID), Администрацията за биомедицински разработки и перспективни изследвания (BARDA) и самата компания AstraZeneca за своите притеснения, става ясно от съобщение, поместено на сайта на американското здравно министерство.
"Призоваваме компанията да прегледа данните за ефективността на ваксината в сътрудничество с DSMB и да гарантира, че в максимално кратък срок се публикуват възможно най-точните и най-новите данни от проведените изпитвания", се казва в изявлението на NIAID.
Ден по-рано пресслужбата на AstraZeneca обяви, че ваксината ѝ срещу коронавируса, разработена от компанията съвместно с Оксфордския университет, е показала висока степен на ефективност в третата фаза на клиничните изпитвания в САЩ, Чили и Перу.
Според компанията ваксината ѝ е ефективна в 79 процента от случаите на симптоматична коронавирусна инфекция и осигурява 100 процента защита срещу тежко заболяване с усложнения и хоспитализация. Съобщено беше също, че сред пациентите на възраст над 65 години ефективността на ваксината е 80 процента.
Компания AstraZeneca посочи още, че експертите ѝ не са установили проблеми с безопасността на ваксината, включително образуването на тромби, което породи опасения в Европа и накара някои страни временно да преустановят използването ѝ.
Ваксината на AstraZeneca е разрешена за употреба в десетки страни, но все още не е одобрена в САЩ.
В прессъобщението се посочваше още, че компанията ще подготви документи, които ще представи в близките седмици пред американското Управление за контрол над хранителните продукти и лекарствата (FDA) за сертифициране на ваксината по ускорена процедура.
Разрешението и насоките за употреба на ваксината в САЩ ще бъдат определени от FDA и Центровете за контрол и профилактика на заболяванията (CDC) след щателен преглед на данните от независими консултативни комисии.
При оценката си дали да разреши някоя ваксина, FDA разглежда данните от най-актуалните изпитвания, отбелязва АП.
Британско-шведската компания каза, че възнамерява да внесе заявката си пред FDA в близките седмици.
Ваксината на AstraZeneca вероятно е много добра, но независимият борд по оценката ѝ има притеснения относно това как фармацевтичната компания е представила данните в прессъобщението си тази седмица, коментира във вторник д-р Антъни Фаучи, главен медицински съветник на Белия дом и директор на NIAID .
"Това вероятно е много добра ваксина. Ако погледнете данните, те са наистина достатъчно добри, но когато са сложени в прессъобщение, не са напълно акуратни", каза той в интервю за ABC News.
Д-р Фаучи уточни, че притесненията на DSMB са породени от това, че публикуваните в съобщението данни са донякъде остарели и може да са малко подвеждащи.
Той изрази съжаление, че случващото се може да добави към обществените съмнения към ваксините и вероятно да доведе до още по-голямо колебание.
Отговорът на AstraZeneca
По-късно във вторник лабораторията AstraZeneca обеща да предостави до 48 часа най-новите си данни на американския регулаторен орган, който следи клиничните тестове и който разкритикува "потенциално остарелите" й данни за ваксината й срещу новия коронавирус, предаде Франс прес.
Компанията обясни в изявление, че е използвала данни отпреди 17 февруари за публикуваните вчера резултати от клиничните тестове в САЩ и че иска незабавно да влезе във връзка с американската комисия за наблюдение на данните и безопасността (DSMB), за да й предостави "анализ с възможно най-актуалните данни".
AstraZeneca ще предостави данни от клиничните тестове на ваксината си в САЩ на Европейската агенция за лекарствата (ЕМА), която може да коригира оценката си за тази ваксина, ако е необходимо, заяви ръководителката на ЕМА Емър Кук, цитирана от Ройтерс.
"Тези клинични тестове показват по-голяма ефикасност (на ваксината), отколкото предишните тестове, които ние наблюдавахме", каза Кук пред Европейския парламент. Тя не коментира текущия спор за остарели данни на АстраЗенека, за които говори американският регулаторен орган.
"Компанията обеща да ни предостави данни и ние ще коригираме оценката си, ако има нова информация, която трябва да се вземе предвид", каза тя.
mediapool.bg

 Близкият изток | Ср, 27 Ноем 2024г. 20:59ч. | Израел ще обжалва международната заповед за арест на Нетаняху
Близкият изток | Ср, 27 Ноем 2024г. 20:59ч. | Израел ще обжалва международната заповед за арест на Нетаняху